在制药、医疗器械等行业中,计算机化系统验证是确保系统符合法规要求、数据完整性与产品质量的关键环节。当您在使用如AutoCAD 2008等软件时遇到“正在验证许可”的提示,这本身也是软件验证与授权管理的一个微观体现,它关联着整个系统验证框架中对于软硬件分类与生命周期的管理。本节将聚焦于计算机化系统的软硬件分类及其开发流程,为深入理解验证实践奠定基础。
一、计算机化系统软硬件分类
根据GAMP 5(良好自动化生产实践指南)等国际公认指南,计算机化系统的软硬件通常基于其复杂程度、定制化水平以及对产品质量的潜在影响进行分类,以便采取相适应的验证与控制策略。
- 硬件分类:
- 标准硬件:如商业现成的服务器、工作站、网络设备、扫描仪等。其验证重点在于安装确认与运行确认,确保其在预定环境中正常工作。
- 定制硬件:为特定工艺或功能量身定制的设备。此类硬件需要更严格的验证,涵盖设计、开发、测试到安装的全过程。
- 软件分类:
- 第1类:基础设施软件:如操作系统、数据库管理系统、网络管理工具。通常通过评估供应商资质与适用性测试进行控制。
- 第2类:不可配置的软件产品:如AutoCAD 2008、Office套件等成熟的商业现成软件。验证重点在于安装确认、版本管理、权限控制(正如“许可验证”所涉及)及功能在黑盒层面的测试,以证明其适用于既定用途。
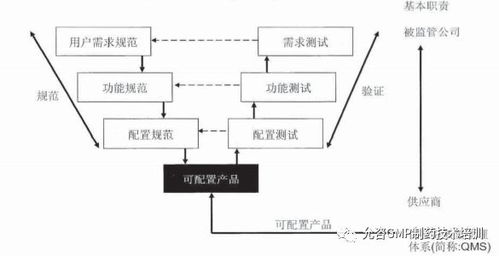
- 第3类:可配置的软件产品:如LIMS(实验室信息管理系统)、ERP系统。除了软件产品本身的评估,还需对配置部分(如工作流程、报告模板)进行详细的验证,确保配置符合用户需求且受控。
- 第4类:定制开发的软件:完全为用户特定需求而开发的软件。这类软件需要最严格的验证活动,贯穿从用户需求说明、功能设计、代码开发、测试到部署的完整生命周期。
- 第5类:定制开发的系统:包含定制硬件和/或定制软件的复杂集成系统。其验证最为复杂,需对整个系统的设计与开发进行全面的生命周期管理。
二、计算机化系统软硬件开发流程
规范的开发流程是确保系统质量、降低验证风险的基础,遵循“质量源于设计”的原则。无论是商业软件的选择还是定制系统的构建,其生命周期管理都包含类似的核心阶段:
- 概念与规划阶段:明确业务目标,定义项目范围与资源。
- 需求定义阶段(URS - 用户需求说明):详细记录用户对系统的所有功能性、性能、合规性与安全性的要求。这是所有后续开发与验证活动的基石。
- 设计与开发阶段:
- 软件:基于需求,进行架构设计、详细设计、编码和单元测试。对于商业软件,此阶段主要由供应商完成,但用户需评估其开发实践是否合规。
- 硬件:进行机械、电气设计,制造原型并进行测试。
- 测试阶段:
- 集成测试:验证软硬件各组件能否正确协同工作。
- 系统测试/功能测试(FAT/SAT):在供应商处(FAT)和用户现场(SAT)对整个系统进行测试,确保其满足用户需求。对于商业软件,这通常表现为在模拟或真实环境中的功能黑盒测试。
- 部署与验收阶段:系统在正式生产环境中的安装、数据迁移、用户培训及最终的验收确认。
- 运维与监控阶段:系统上线后的日常使用、变更管理、备份恢复、性能监控与定期回顾。
- 退役阶段:系统生命周期结束时的数据归档与系统停用。
三、分类与开发流程对验证的意义
对软硬件进行分类,核心目的在于实施基于风险、比例相称的验证策略。例如,对于AutoCAD 2008这样的第2类软件,我们无需审查其源代码,但必须通过严格的测试证明其“绘图”、“标注”等功能在特定使用场景下稳定可靠,并且其许可管理机制能防止未授权使用。而对于一个定制的生产控制系统(第4或5类),则必须深入参与其设计评审、代码审核,并进行全面的测试。
理解并遵循结构化的开发流程,则能确保从需求源头开始就植入质量要素,使验证活动不再是项目末期的“附加任务”,而是贯穿始终的质量保证过程。这不仅有助于高效通过法规检查,更能从根本上保障系统的可靠性、数据的完整性,最终服务于产品安全与患者健康。
而言,“计算机化系统验证”并非一个孤立的活动,它始于对系统组件(软硬件)的清晰分类,并紧密嵌入于系统的整个开发与生命周期管理流程之中。只有将分类管理、规范开发与风险控制相结合,才能构建起坚实可靠的合规性体系。